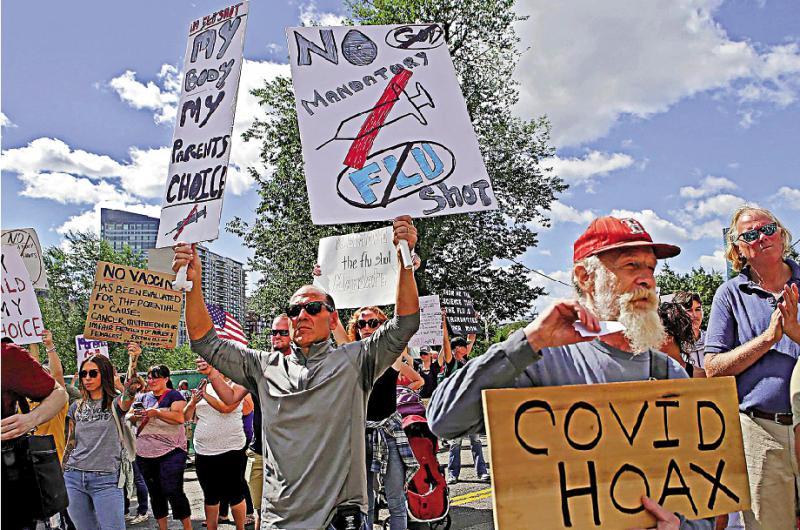
图:美国部分民众并不信任疫苗,是大规模注射计劃的又一阻碍/美联社
【大公报讯】综合美联社、《华尔街日报》、美国广播公司报道:美国藥厂辉瑞20日宣布,已就其与德国BioNTech公司共同研发的新冠疫苗,向美国食品和藥物管理局(FDA)提出紧急使用授权申请,预计最快下月就能供应首批疫苗。美国藥厂莫德纳(Moderna)料将很快跟进。这两家藥厂近期“喜讯”频传,旗下新冠疫苗均号称安全与有效性兼备,但有报道指出,试验并未考虑潜在无症状感染者,实际效果恐不如预期。此外,即便FDA以最快速度批准紧急使用授权,疫苗生产、分配等环节仍有很多问题需要解决。
辉瑞18日公布疫苗三期试验最新结果,称其有效性达95%,且并无严重副作用。20日,该公司表示,疫苗有效性和安全性兼备,能够达到FDA紧急使用授权标準。辉瑞执行总裁布拉发表声明称,在疫情肆虐全球的背景下,“我们提供安全有效疫苗的工作从未如此紧迫”。辉瑞亦开始在欧盟、英国等地推动类似申请。
美国总统特朗普选前曾施压藥厂“赶製”疫苗,这加剧民众对疫苗的不信任。美国顶级传染病专家福奇20日强调,虽然辉瑞和莫德纳几个月内就完成了以往需花费数年的疫苗研发工作,但过程中并未牺牲安全性或科学性。
试验未考虑无症状患者
接到辉瑞申请后,FDA将启动一系列流程。首先,FDA科学家将评估辉瑞提供的疫苗数据的準确性,仅此环节就可能持续两至三周。大约在12月初,美国主要学术中心医生组成的FDA独立顾问小组,将基於FDA内部分析,就疫苗安全性及有效性展开辩论,例如该疫苗是否对特定种族或年龄群体有效等,并就是否批准使用该疫苗、应该在哪些人群中使用提出建议。
在FDA顾问的会议上,公众将首次见到疫苗具体试验数据。迄今为止,关於疫苗的信息均来自辉瑞和BioNTech的声明。他们声称170名染疫受试者中,仅有8人属於注射疫苗的试验组,有效性高达95%。
然而,美联社等媒体指出,辉瑞和莫德纳均只统计出现症状并确诊的志愿者,并未考虑出现无症状感染者的情况。疫情出现以来,全球各国均发现大量无症状感染者,且能够传染他人。现在无法排除注射了辉瑞疫苗,仍会成为无症状感染者并播毒的可能。
若FDA在考虑顾问建议后,决定批准紧急使用授权,美国疾控中心顾问小组将负责决定谁先获得注射机会。美媒指,紧急使用授权并非正式许可,辉瑞必须向使用者提供阐明潜在风险的说明。另外,由於试验中没有招募孕妇志愿者,这一群体暂时不会被允许注射疫苗。
莫德纳上月才启动生产
据报道,由於初期供应有限,疫苗料将优先被提供给一线医护人员、长者等高风险群体。“曲速行动”计劃副主管威克表示,初期人们只能到医院和大型医疗中心注射疫苗。普通民众需等待数月,才能在当地藥房注射。
辉瑞宣布将在年底前向全球供应5000万剂疫苗。根据美国国家医学会公布的数据,美国12月将获得2500万剂,明年1月获得3000万剂,2至3月再获得3500万剂。然而,英国广播公司指出,量产疫苗并不是简单地放大实验室微量生产过程,大规模生产往往会出现无法预料的情况。FDA前疫苗主管贝勒警告,藥厂宣布的产量仅仅是预测,“这不像做薄饼,生产疫苗非常複杂”。另外,辉瑞疫苗需在零下70摄氏度的极度低温条件下储存和运输,亦是一大难题。
与莫德纳合作的瑞士藥厂隆察亦表示,时间和人手都是很大挑战。他们上月才启动生产线,目前仍在生产首批藥物,且测试设备、培训人手均需要时间。